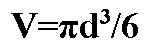Kaip surasti dujų kiekį?

Prieš sprendžiant problemas, būtina atsižvelgti į formules irTaisyklės, kaip surasti dujų kiekį. Reikėtų prisiminti Avogadro įstatymą. Ir paties dujų kiekį galima apskaičiuoti naudojant keletą formulių, pasirenkant iš jų tinkamą. Renkantis reikiamą formulę labai svarbios aplinkos sąlygos, ypač temperatūra ir slėgis.
Avogadro įstatymas
Tai sako, kad tuo pačiu spaudimu irtas pats temperatūra, vienodi kiekiai to įvairių dujų, bus turi tą patį numerį molekulių. Prijungimo prie gamtinių dujų molekulių kiekis šiose vienu moliu, yra Avogadro skaičius. Dėl to, kad teisės, tai reiškia, kad: 1 kmol (kmol) idealios dujų, ir bet koks, tuo pačiu slėgio ir temperatūros (760 mm Hg t = 0 ° C) visada užima tūris = 22.4136 m3.
Kaip nustatyti dujų kiekį
- Dažniausiai randama formulė V = n * Vmužduotys. Čia, dujų srauto litrais - V, VM - molinis dujų tūris (L / mol), kuris normaliomis sąlygomis = 22,4 l / mol, ir n - medžiagos kiekis mol. Kai pagal ne dėl medžiagos kiekio, bet yra svorio medžiaga, tada mes taip: n = m / M. Čia M yra g / mol (cheminės medžiagos molinė masė), o medžiagos masė gramais yra m. Periodinėje lentelėje parašyta po kiekvienu elementu, kaip jo atominė masė. Mes pridedame visas mases ir surenkite reikalingą.
- Taigi, kaip apskaičiuoti dujų kiekį. Kad užduotis druskos rūgštimi, siekiant ištirpinti 10 g aliuminio. Klausimas: kiek vandenilio gali išsiskirti, kai n. y.? Reakcijos lygtis yra taip: 2AL + 6HCl (Gage.) = 2AlCl3 + 3H2. Pradžioje, mes rasti aliuminio (skaičius) apimanti paviršiuje reaguojantį pagal formulę: n (Al) = m (Al), / M (Al),. aliuminio svoris (molinis) yra paimtas iš periodinės lentelės M (Al) = 27g / mol. Pakeičiame: n (Al) = 10/27 = 0,37 mol. Iš chemijos lygtį akivaizdžiu, 3 molių vandenilio yra suformuota ištirpinant 2 mol aliuminio. Ji turėtų būti apskaičiuojamas, ir kiek vandenilis išryškina 0,4 molių aliuminio: n (H2) = 3 * 0.37 / 2 = 0,56mol. Mes pakeičiame duomenis formulėje ir randame šių dujų kiekį. V = N * Vm = 0,56 * 22,4 = 12,54l.